अभिक्रिया की दिशा और पदार्थों की सांद्रता में बदलाव को दर्शाने वाली मात्रात्मक विशेषता को रासायनिक प्रतिक्रिया का संतुलन स्थिरांक कहा जाता है। संतुलन स्थिरांक तापमान और अभिकारकों की प्रकृति पर निर्भर करता है।
प्रतिवर्ती और अपरिवर्तनीय प्रतिक्रियाएं
सभी प्रतिक्रियाओं को दो प्रकारों में विभाजित किया जा सकता है:
- प्रतिवर्ती, एक साथ दो परस्पर विपरीत दिशाओं में बहना;
- अचलकम से कम एक प्रारंभिक पदार्थ की कुल खपत के साथ एक ही दिशा में बहना।
अपरिवर्तनीय प्रतिक्रियाओं में, अघुलनशील पदार्थ आमतौर पर एक अवक्षेप या गैस के रूप में बनते हैं। इन प्रतिक्रियाओं में शामिल हैं:
- दहन:
सी 2 एच 5 ओएच + 3 ओ 2 → 2सीओ 2 + एच 2 ओ;
- अपघटन:
2केएमएनओ 4 → के 2 एमएनओ 4 + एमएनओ 2 + एच 2 ओ;
- एक अवक्षेप या गैस के निर्माण के साथ संबंध:
BaCl 2 + Na 2 SO 4 → BaSO 4 ↓ + 2NaCl।

चावल। 1. BaSO 4 की वर्षा।
प्रतिवर्ती प्रतिक्रियाएं केवल कुछ निश्चित परिस्थितियों में ही संभव हैं। मूल पदार्थ एक नया पदार्थ देते हैं, जो तुरंत अपने घटक भागों में टूट जाता है और फिर से एकत्र हो जाता है। उदाहरण के लिए, प्रतिक्रिया के परिणामस्वरूप 2NO + O 2 ↔ 2NO 2 नाइट्रिक ऑक्साइड (IV) आसानी से नाइट्रिक ऑक्साइड (II) और ऑक्सीजन में विघटित हो जाता है।
संतुलन
एक निश्चित समय के बाद, प्रतिवर्ती प्रतिक्रिया की दर धीमी हो जाती है। रासायनिक संतुलन हासिल किया जाता है - एक ऐसी स्थिति जिसमें समय के साथ शुरुआती पदार्थों और प्रतिक्रिया उत्पादों की एकाग्रता में कोई बदलाव नहीं होता है, क्योंकि आगे और पीछे की प्रतिक्रियाओं की दर बराबर होती है। संतुलन केवल सजातीय प्रणालियों में ही संभव है, अर्थात सभी प्रतिक्रियाशील पदार्थ या तो तरल पदार्थ या गैस होते हैं।
आयोडीन के साथ हाइड्रोजन की बातचीत की प्रतिक्रिया के उदाहरण पर रासायनिक संतुलन पर विचार करें:
- सीधी प्रतिक्रिया -
एच 2 + आई 2 ↔ 2HI;
- पीछे की प्रतिक्रिया -
2HI एच 2 + आई 2।
जैसे ही दो अभिकर्मक मिश्रित होते हैं - हाइड्रोजन और आयोडीन - हाइड्रोजन आयोडीन अभी तक मौजूद नहीं है, क्योंकि साधारण पदार्थ केवल प्रतिक्रिया करते हैं। बड़ी संख्या में प्रारंभिक पदार्थ एक दूसरे के साथ सक्रिय रूप से प्रतिक्रिया करते हैं, इसलिए प्रत्यक्ष प्रतिक्रिया की दर अधिकतम होगी। इस मामले में, रिवर्स प्रतिक्रिया आगे नहीं बढ़ती है, और इसकी दर शून्य है।
प्रत्यक्ष प्रतिक्रिया की दर को ग्राफिक रूप से व्यक्त किया जा सकता है:
पीआर = के पीआर ∙ ,
जहाँ k pr प्रत्यक्ष प्रतिक्रिया की दर स्थिरांक है।
समय के साथ, अभिकर्मकों का सेवन किया जाता है, उनकी एकाग्रता कम हो जाती है। तदनुसार, आगे की प्रतिक्रिया की दर कम हो जाती है। उसी समय, एक नए पदार्थ, हाइड्रोजन आयोडाइड की सांद्रता बढ़ जाती है। जमा होने पर, यह विघटित होना शुरू हो जाता है, और रिवर्स रिएक्शन की दर बढ़ जाती है। इसे के रूप में व्यक्त किया जा सकता है
गिरफ्तारी = कश्मीर गिरफ्तारी ∙ 2।
हाइड्रोजन आयोडाइड चुकता है, क्योंकि अणु का गुणांक दो है।
कुछ बिंदु पर, आगे और पीछे की प्रतिक्रियाओं की दर बराबर होती है। रासायनिक संतुलन की स्थिति होती है।

चावल। 2. प्रतिक्रिया दर बनाम समय का ग्राफ।
संतुलन को या तो प्रारंभिक सामग्री की ओर या प्रतिक्रिया के उत्पादों की ओर स्थानांतरित किया जा सकता है। बाह्य कारकों के प्रभाव में विस्थापन को ले चेटेलियर का सिद्धांत कहा जाता है। संतुलन किसी एक पदार्थ के तापमान, दबाव, सांद्रता से प्रभावित होता है।
लगातार गणना
संतुलन की स्थिति में, दोनों प्रतिक्रियाएं आगे बढ़ती हैं, लेकिन साथ ही, पदार्थों की सांद्रता संतुलन में होती है (संतुलन सांद्रता बनती है), क्योंकि दरें संतुलित होती हैं (ν pr \u003d ν arr)।
रासायनिक संतुलन को रासायनिक संतुलन स्थिरांक की विशेषता है, जिसे सारांश सूत्र द्वारा व्यक्त किया जाता है:
के पी \u003d के पीआर / के एआर \u003d कास्ट।
प्रतिक्रिया दर स्थिरांक को प्रतिक्रिया दर अनुपात के रूप में व्यक्त किया जा सकता है। आइए रिवर्स रिएक्शन का सशर्त समीकरण लें:
एए + बीबी सीसी + डीडी।
फिर आगे और पीछे की प्रतिक्रियाओं की दर बराबर होगी:
- ν इंक = के इंक [ए] पी ए ∙ [बी] पी बी
- ν गिरफ्तारी = कश्मीर गिरफ्तारी ∙ [सी] पी सी ∙ [डी] पी डी।
तदनुसार, यदि
पीआर \u003d ν गिरफ्तार,
के पूर्व ∙ [ए] पी ए ∙ [बी] पी बी = के गिरफ्तारी ∙ [सी] पी सी ∙ [डी] पी डी।
यहाँ से हम अचरों का अनुपात व्यक्त कर सकते हैं:
के एआर / के इंक = [सी] पी सी ∙ [डी] पी डी / [ए] पी ए ∙ [बी] पी बी।
यह अनुपात संतुलन स्थिरांक के बराबर है:
के पी = [सी] पी सी ∙ [डी] पी डी / [ए] पी ए ∙ [बी] पी बी।

चावल। 3. संतुलन स्थिरांक का सूत्र।
मान दर्शाता है कि अग्र अभिक्रिया की दर, प्रतिवर्ती अभिक्रिया की दर से कितनी गुना अधिक है।
हमने क्या सीखा?
अंतिम उत्पादों के आधार पर प्रतिक्रियाओं को प्रतिवर्ती और अपरिवर्तनीय में वर्गीकृत किया जाता है। प्रतिवर्ती प्रतिक्रियाएं दोनों दिशाओं में आगे बढ़ती हैं: प्रारंभिक सामग्री अंतिम उत्पाद बनाती है, जो प्रारंभिक पदार्थों में विघटित होती है। एक प्रतिक्रिया के दौरान, आगे और पीछे की प्रतिक्रियाओं की दर संतुलित होती है। इस अवस्था को रासायनिक संतुलन कहते हैं। इसे प्रतिक्रिया उत्पादों के संतुलन सांद्रता के उत्पाद के अनुपात के रूप में प्रारंभिक सामग्रियों के संतुलन सांद्रता के उत्पाद के रूप में व्यक्त किया जा सकता है।
विषय प्रश्नोत्तरी
रिपोर्ट मूल्यांकन
औसत रेटिंग: 4.8. प्राप्त कुल रेटिंग: 272।
रसायन विज्ञान में, संतुलन राज्य अधिकांश गैसीय और तरल प्रणालियों के साथ-साथ कठोर मिश्र धातुओं के एक बड़े समूह की विशेषता है। इसलिए, रासायनिक संतुलन के नियम बहुत व्यावहारिक महत्व के हैं। गिब्स ऊर्जा के लिए समीकरण का विश्लेषण करते समय, यह पाया जाता है कि थर्मोडायनामिक सिस्टम में राज्य उत्पन्न हो सकते हैं जब विपरीत रूप से निर्देशित प्रक्रियाएं एक साथ होती हैं, लेकिन पूरे सिस्टम की स्थिति संतुलन में रहती है, यानी। इसके पैरामीटर अपरिवर्तित हैं (ए = 0)। हालांकि, समय में प्रणाली के मापदंडों की स्थिरता सही रासायनिक संतुलन के लिए एक आवश्यक लेकिन पर्याप्त स्थिति नहीं है। कुछ शर्तों के तहत, सिस्टम के पैरामीटर जिसमें प्रकार की प्रतिक्रियाएं होती हैं
उदाहरण के लिए, वायु के साथ गैसीय अमोनिया का मिश्रण समय के साथ अपरिवर्तित रहता है। हालाँकि, यह एक गर्म उत्प्रेरक - क्रोमियम ऑक्साइड Cr 2 O e - को इस मिश्रण में पेश करने के लिए पर्याप्त है, जैसे ही प्रतिक्रिया शुरू होती है, जिससे नाइट्रोजन डाइऑक्साइड M0 2 का निर्माण होता है: 
गिब्स-हेल्महोल्ट्ज़ समीकरण के अनुसार गणना से पता चलता है कि इस प्रतिक्रिया के लिए एजी 2 ° 98 0 और यह प्रकार (11.1) की प्रतिक्रियाओं से संबंधित है। तो, इस मामले में, हम साथ काम नहीं कर रहे हैं सही संतुलनप्रणाली में, लेकिन केवल बाधित (मेटास्टेबल) अवस्था।
वास्तव में संतुलन प्रणाली का वर्णन करने वाली मॉडल प्रतिक्रिया होगी
वास्तव में संतुलन सजातीय प्रणाली का एक विशिष्ट उदाहरण दो लवणों से तैयार एक जलीय घोल है: लोहा (III) क्लोराइड FeCl 3 और पोटेशियम थायोसाइनेट KCNS और चार पदार्थ युक्त। संकेतित अभिकर्मकों के अलावा, इसमें दो प्रतिक्रिया उत्पाद भी शामिल हैं - आयरन थायोसाइनेट) Fe (CNS) 3 और पोटेशियम क्लोराइड KSL:
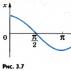
इस प्रकार की अभिक्रिया कहलाती है काइनेटिक रूप से उल्टा,चूंकि वे सिस्टम के किसी भी राज्य में आगे और विपरीत दिशा में दोनों दिशाओं में प्रवाहित होते हैं। मापदंडों की श्रेणी में, जब आगे और पीछे की प्रतिक्रियाओं की दर समान हो जाती है, तो सिस्टम भी थर्मोडायनामिक रूप से प्रतिवर्ती हो जाता है। इसलिए, कोई अक्सर ऐसी प्रतिक्रियाओं की उत्क्रमणीयता की बात करता है, यह निर्दिष्ट किए बिना कि किस प्रकार की प्रतिवर्तीता का मतलब है। जिन प्रणालियों में (11.1) और (11.2) प्रकार की प्रतिक्रियाएं होती हैं, उनमें गिब्स ऊर्जा में परिवर्तन को एक आरेख (चित्र 11.2) द्वारा दर्शाया जा सकता है।

चावल। 11.2.
आरेख का भुज अक्ष प्रणाली की संरचना को दर्शाता है (यह शुद्ध अभिकर्मकों ए से बदलता है; बी प्रारंभिक (प्रारंभिक) अवस्था में, शुद्ध प्रतिक्रिया उत्पादों पी में; पी अंतिम (कॉन) अवस्था में) एक्स के मोल अंशों में, प्रत्येक घटक, और समन्वय अक्ष पर - मूल्य वर्तमान संरचना के मिश्रण के लिए गिब्स ऊर्जा। आरेख से निम्नानुसार है, प्रकार (11.1) की प्रतिक्रिया के लिए, संरचना पर गिब्स ऊर्जा की निर्भरता मोनोटोनिक है। जैसे-जैसे प्रक्रिया आगे बढ़ती है, सिस्टम का मान C घटता जाता है, और मान D, C (इंडेक्स .) जीइस बात पर जोर देता है कि रासायनिक प्रतिक्रिया के लिए गिब्स ऊर्जा में यह परिवर्तन), प्रारंभिक और अंतिम अवस्थाओं में गिब्स ऊर्जा के बीच के अंतर के बराबर, हमेशा नकारात्मक होता है।
(11.2) प्रकार की प्रतिक्रिया के लिए, चित्र अलग है। इस आरेख में सिस्टम का मान C न्यूनतम है, और संपूर्ण आरेख को दो क्षेत्रों में विभाजित किया गया है: बिंदु के बाईं ओर जेडजैसे-जैसे प्रक्रिया आगे बढ़ती है, मान ts.fi(प्रत्यक्ष (पीआर) प्रतिक्रिया के लिए गिब्स ऊर्जा में परिवर्तन) नकारात्मक है, और बिंदु के दाईं ओर जेडजैसे-जैसे प्रक्रिया आगे बढ़ती है, AG का मान ऋणात्मक होता है (? arr (रिवर्स (arr) प्रतिक्रिया के लिए गिब्स ऊर्जा में परिवर्तन)। बिंदु जेडसंतुलन बिंदु है - इसमें और ए जी सी पीआर, और ए; .C oG)p शून्य के बराबर हैं। एक बिंदु पर प्रणाली की संरचना जेडबुलाया संतुलित रचना।एक बिंदु पर संतुलन की स्थिति जेडरासायनिक ऊष्मप्रवैगिकी में यह एक विशेष मूल्य की विशेषता है - निरंतर संतुलन
सियायारवन-
प्रणाली की स्थिति के लिए संतुलन स्थिरांक स्थिर तापमानवहाँ है लगातारमूल्य। संतुलन स्थिरांक को प्रणाली के विभिन्न मापदंडों के संदर्भ में व्यक्त किया जा सकता है, जो सूचकांकों द्वारा परिलक्षित होता है: कश्मीर(दाढ़ सांद्रता के माध्यम से), कश्मीर x(तिल अंशों के माध्यम से), कश्मीर(आंशिक दबावों के माध्यम से), आदि। संतुलन स्थिरांक के लिए एक अभिव्यक्ति के निर्माण के लिए एल्गोरिथ्म सरल है: यह एक अंश के बराबर है, जिसके अंश में संतुलन मापदंडों (एकाग्रता, आंशिक दबाव, तिल अंश, आदि) का उत्पाद है। ।) संबंधित पदार्थों के स्टोइकोमेट्रिक गुणांक के बराबर शक्तियों में प्रतिक्रिया उत्पादों की, और हर में - अभिकर्मकों के लिए एक समान उत्पाद।
अभिव्यक्ति पर विचार करें ![]() मॉडल प्रतिक्रिया (11.2) के लिए:
मॉडल प्रतिक्रिया (11.2) के लिए:
वर्गाकार कोष्ठकों में संलग्न पदार्थ का सूत्र निकाय में पदार्थ की मोलर सांद्रता को दर्शाता है। जब संदर्भ से यह स्पष्ट हो जाता है कि हम संतुलन की स्थिति के बारे में बात कर रहे हैं, तो सूचकांक "बराबर" को छोड़ दिया जाता है। विषमांगी प्रणालियों के मामले में संतुलन स्थिरांक लिखने के रूप की विशेषताओं पर इस अध्याय में बाद में विचार किया जाएगा। यदि निकाय का कोई घटक ठोस है, तो उसकी सांद्रता एक स्थिर मान है, इसे बाईं ओर स्थानांतरित किया जाता है और संतुलन स्थिरांक में शामिल किया जाता है। इस मामले में, विश्लेषणात्मक अभिव्यक्ति में ऐसे घटक का प्रतिनिधित्व नहीं किया जाता है।
विश्लेषणात्मक रूप से, विभिन्न प्रकार के संतुलन स्थिरांक एक दूसरे से इस प्रकार संबंधित हैं:
उसी समय, कोई फर्क नहीं पड़ता कि K को कैसे व्यक्त किया जाता है, यह सिस्टम का एक पैरामीटर है और बिंदु की स्थिति पर निर्भर नहीं करता है जेडयह बिंदु गतिशील है और प्रणाली की तैयारी की विधि पर निर्भर करता है, जिसे प्रयोगात्मक रूप से सत्यापित किया जा सकता है। यदि आप प्रारंभिक अवस्था में घटकों के अनुपात को बदलते हैं, उदाहरण के लिए, सिस्टम में घटक O और E (प्रतिक्रिया उत्पाद) जोड़ें, तो बिंदु की स्थिति जेडबाईं ओर शिफ्ट हो जाएगा, लेकिन यदि आप घटक ए और बी (अभिकर्मक) जोड़ते हैं, तो दाईं ओर। नीचे हम के आधार पर प्रणाली के संतुलन बिंदु की स्थिति में इस तरह के बदलाव पर विचार करते हैं ले चेटेलियर-ब्राउन सिद्धांत।
संतुलन स्थिरांक आयामी और आयामहीन मात्रा दोनों हो सकते हैं। संतुलन स्थिरांक का आयाम उस मात्रा के आयाम से निर्धारित होता है जिसके माध्यम से इसे व्यक्त किया जाता है (एकाग्रता, आंशिक दबाव, आदि), और इस आयाम के बराबर है जो अंतिम और प्रारंभिक के गुणांक के बीच अंतर के बराबर है। प्रतिक्रिया के घटक: ![]()
संतुलन स्थिरांक को एक अंश के रूप में लिखा जाता है, जिसके अंश में प्रतिक्रिया उत्पादों के पैरामीटर शामिल होते हैं, और हर - प्रारंभिक पदार्थों के पैरामीटर। संतुलन स्थिरांक को मोल भिन्नों के रूप में व्यक्त करना सबसे सुविधाजनक है (इस मामले में, इसका कोई आयाम नहीं है):
![]()
गैसीय घटकों को शामिल करने वाली प्रक्रियाओं के लिए, गैसीय घटकों के आंशिक दबावों के संदर्भ में संतुलन स्थिरांक को व्यक्त करना सुविधाजनक है:
![]()
दाढ़ सांद्रता के संदर्भ में संतुलन स्थिरांक की अभिव्यक्ति स्थिर मात्रा में या समाधान में प्रक्रियाओं के लिए सुविधाजनक है (यदि समाधान की मात्रा व्यावहारिक रूप से स्थिर रहती है):
![]()
यदि प्रक्रिया मोलों की संख्या (Dy = 0) को बदले बिना चलती है, तो संतुलन स्थिरांक के सभी व्यंजक मेल खाते हैं: ![]()
इस मामले में, सभी संतुलन स्थिरांक आयामहीन हो जाते हैं।
आइए हम प्रतिवर्ती रासायनिक प्रतिक्रियाओं (सामान्य रूप में) के लिए संतुलन स्थिरांक प्राप्त करें
प्रतिक्रिया दर:
हम समीकरण के बाईं ओर स्थिरांक (दर स्थिरांक) को स्थानांतरित करते हैं, और चर (एकाग्रता) को समीकरण के दाईं ओर स्थानांतरित करते हैं, अर्थात। हम इस समानता को अनुपात के रूप में लिखते हैं:
स्थिरांक के व्यंजक में अभिक्रिया समीकरण में पदार्थ के सामने गुणांकों के बराबर घातों में लिए गए पदार्थों की साम्यावस्था सांद्रता शामिल है।
संतुलन स्थिरांक प्रक्रिया की गहराई को दर्शाता है। संतुलन स्थिरांक का मान जितना अधिक होगा, संतुलन के क्षण में प्रतिक्रिया उत्पादों की सांद्रता उतनी ही अधिक होगी, अर्थात। प्रतिक्रिया जितनी अधिक पूर्ण होगी।
संतुलन स्थिरांक अभिकारकों की प्रकृति पर निर्भर करता है, लेकिन उत्प्रेरक की उपस्थिति पर निर्भर नहीं करता है, क्योंकि यह आगे और पीछे दोनों प्रतिक्रियाओं को समान रूप से तेज करता है। संतुलन स्थिरांक के मूल्य पर अन्य कारकों (पदार्थों की सांद्रता, गैस के दबाव और तापमान) के प्रभाव का विश्लेषण विशिष्ट उदाहरणों का उपयोग करके नीचे किया जाएगा।
विशिष्ट उदाहरणों पर संतुलन स्थिरांक के व्यंजक की व्युत्पत्ति पर विचार करें।
उदाहरण 2प्रतिक्रिया के लिए: एन 2(जी) +3एच 2(जी) Û 2एनएच 3(जी)
वी पीआर \u003d के 1 3; वी गिरफ्तार। = कश्मीर 2 2।यदि एक वी पीआर \u003d वी गिरफ्तारी। ,फिर के 1 [एच 2] 3 = के 2 2 ,
 .
.
यदि ठोस पदार्थ प्रतिक्रिया (विषम प्रणाली) में भाग लेते हैं, तो उनकी एकाग्रता प्रतिक्रिया दर की अभिव्यक्ति में शामिल नहीं होती है (क्योंकि यह प्रति इकाई सतह प्रति इकाई समय पर स्थिर रहती है), और इसलिए संतुलन स्थिरांक।
उदाहरण 3प्रतिक्रिया के लिए: सी (टीवी।) + ओ 2 (जी) सीओ 2 (जी)रासायनिक संतुलन स्थिरांक के बराबर होगा ![]() .
.
उदाहरण 4एक प्रतिवर्ती रासायनिक प्रतिक्रिया में ए + 2 बी Û सीसंतुलन निम्नलिखित संतुलन सांद्रता में हुआ: [ए] = 0.6 मोल/ली; [बी] = 1.2 मोल/ली; [सी] = 2.16 मोल/ली। संतुलन स्थिरांक और पदार्थ की प्रारंभिक सांद्रता निर्धारित करें लेकिनतथा पर.
सभी रासायनिक प्रतिक्रियाओं को विभाजित किया जा सकता है प्रतिवर्तीतथा अपरिवर्तनीय।प्रतिवर्ती प्रतिक्रियाएं वे हैं जो एक निश्चित तापमान पर दो विपरीत दिशाओं में ध्यान देने योग्य दर से आगे बढ़ती हैं - आगे और पीछे। प्रतिवर्ती प्रतिक्रियाएं अंत तक नहीं चलती हैं, कोई भी अभिकारक पूरी तरह से भस्म नहीं होता है। एक उदाहरण प्रतिक्रिया है
एक निश्चित तापमान सीमा में, यह प्रतिक्रिया प्रतिवर्ती है। संकेत " » प्रतिवर्तीता का प्रतीक है।
अपरिवर्तनीय प्रतिक्रियाएं वे प्रतिक्रियाएं हैं जो केवल एक दिशा में अंत तक जाती हैं, अर्थात। अभिकारकों में से एक के पूर्ण उपभोग तक। एक अपरिवर्तनीय प्रतिक्रिया का एक उदाहरण पोटेशियम क्लोरेट का अपघटन है:
सामान्य परिस्थितियों में पोटेशियम क्लोराइड और ऑक्सीजन से पोटेशियम क्लोरेट का निर्माण असंभव है।
रासायनिक संतुलन की स्थिति। रासायनिक संतुलन स्थिरांक
आइए हम कुछ उत्क्रमणीय अभिक्रियाओं के समीकरण को सामान्य रूप में लिखें:
प्रतिक्रिया शुरू होने तक, प्रारंभिक पदार्थ ए और बी की सांद्रता अधिकतम थी। प्रतिक्रिया के दौरान, उनका सेवन किया जाता है और उनकी एकाग्रता कम हो जाती है। इस मामले में, सामूहिक कार्रवाई के नियम के अनुसार, प्रत्यक्ष प्रतिक्रिया की दर
घटेगा। (इसके बाद, शीर्ष पर तीर प्रक्रिया की दिशा को इंगित करता है।) प्रारंभिक क्षण में, प्रतिक्रिया उत्पादों डी और ई की सांद्रता शून्य के बराबर थी। प्रतिक्रिया के दौरान, वे बढ़ जाते हैं, रिवर्स प्रतिक्रिया की दर समीकरण के अनुसार शून्य से बढ़ जाती है:
अंजीर पर। 4.5 आगे और पीछे की गति में परिवर्तन दिखाता है
समय के साथ प्रतिक्रियाएं। समय t के बाद, ये गतियाँ समान हैं - - " 
चावल। 4.5.समय में प्रत्यक्ष (1) और रिवर्स (2) प्रतिक्रियाओं की दर में परिवर्तन: - उत्प्रेरक की अनुपस्थिति में: ......... - उत्प्रेरक की उपस्थिति में
इस अवस्था को रासायनिक संतुलन कहते हैं। रासायनिक संतुलन सहज प्रक्रियाओं की सबसे स्थिर, सीमित अवस्था है।यह अनिश्चित काल तक जारी रह सकता है यदि बाहरी स्थितियों को नहीं बदला जाता है। संतुलन की स्थिति में पृथक प्रणालियों में, सिस्टम की एन्ट्रॉपी अधिकतम तक पहुंच जाती है और स्थिर रहती है, अर्थात। डीएस = 0. समदाबीय-समतापीय स्थितियों के तहत, प्रक्रिया की प्रेरक शक्ति, संतुलन पर गिब्स ऊर्जा, न्यूनतम मान लेती है और आगे नहीं बदलती है, अर्थात। डीजी = 0.
संतुलन की स्थिति में प्रतिक्रिया में प्रतिभागियों की सांद्रता को संतुलन कहा जाता है।एक नियम के रूप में, उन्हें वर्ग कोष्ठक में संलग्न संबंधित पदार्थों के सूत्रों द्वारा निरूपित किया जाता है, उदाहरण के लिए, अमोनिया की संतुलन एकाग्रता प्रारंभिक, गैर-संतुलन एकाग्रता C ^ NH ^ के विपरीत निरूपित की जाती है।
चूंकि संतुलन की स्थिति में प्रत्यक्ष और विपरीत प्रक्रियाओं की दर समान होती है, इसलिए हम समीकरणों के सही भागों (4.44) को समान करते हैं और
- -^ मैं-
- (4.45), सांद्रता के पदनाम की जगह: ए: [ए]""[बी]" =?[डी] /; = 1 एटीएम)। CO के 1 mol और H2O के 5 mol वाले मिश्रण को इस तापमान पर गर्म किया गया। संतुलन मिश्रण में पानी के मोल अंश की गणना करें।
4 विकल्प
1 . आंशिक दबाव के प्रत्यक्ष माप द्वारा संतुलन स्थिरांक का मान निर्धारित करने की एक विधि का वर्णन करें।
2. गैसीय पदार्थों ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 0.5 ए + बी \u003d सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। प्रारंभिक समय में, कोई नहीं है प्रणाली में प्रतिक्रिया उत्पाद, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.3 के बराबर होती है, और कुल दबाव 1.5 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 । प्रतिक्रिया का संतुलन स्थिरांक N2O4 (g) \u003d 2NO2 (g) 25 ° C पर 0.143 ([p] \u003d 1 atm) है। इस तापमान पर 1 ग्राम N2O4 युक्त 1 लीटर के बर्तन में स्थापित होने वाले दबाव की गणना करें।
5 विकल्प
1 . आप प्रयोग का सहारा लिए बिना किसी अभिक्रिया के साम्य स्थिरांक का मान कैसे निर्धारित कर सकते हैं?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 0.5 ए + 3 बी = सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। प्रारंभिक समय में कोई प्रतिक्रिया नहीं होती है सिस्टम में उत्पाद, और शुरुआती सामग्री मात्रा में ली जाती है। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.3 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . 1.79·10 -2 mol I2 युक्त एक 3-लीटर के बर्तन को 973 K तक गर्म किया गया। संतुलन पर बर्तन में दबाव 0.49 atm निकला। आदर्श गैसों को मानकर, प्रतिक्रिया के लिए 973 K पर संतुलन स्थिरांक की गणना करें
I2(r) = 2I(r)।
6 विकल्प
1. पहले से अज्ञात तापमान पर रासायनिक संतुलन स्थिरांक के मूल्य को निर्धारित करने के लिए प्रतिक्रिया आइसोबार समीकरण का उपयोग करना।
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 3 ए + बी = सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। प्रारंभिक समय में, कोई प्रतिक्रिया उत्पाद नहीं होता है प्रणाली में, और प्रारंभिक पदार्थों को स्टोइकोमेट्रिक मात्रा में लिया जाता है। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.4 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . प्रतिक्रिया के लिए PCl5(g) =PCl3(g) +Cl2(g) 250 डिग्री सेल्सियस पर, गिब्स ऊर्जा में मानक दाढ़ परिवर्तन = - 2508 J/mol। 250 °C पर PCl5 के PCl3 और Cl2 में रूपांतरण की डिग्री किस कुल दबाव पर 30% होगी?
7 विकल्प
1. जिस प्रणाली में एंडोथर्मिक गैस-चरण प्रतिक्रिया ए + 3 बी = 2 सी होती है वह 400 के और 5 एटीएम पर संतुलन में होती है। यदि गैसें आदर्श हैं, तो स्थिर आयतन पर अक्रिय गैस मिलाने से उत्पाद की उपज कैसे प्रभावित होगी?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 2 ए + बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.3 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . प्रतिक्रिया 2HI(g) = H2 + I2(g) के लिए, संतुलन स्थिरांक है केपी\u003d 0.0183 ([p] \u003d 1 atm) 698.6 K पर। तीन लीटर के बर्तन में I2 के 10 ग्राम और H2 के 0.2 ग्राम को इस तापमान पर गर्म करने पर कितने ग्राम HI बनते हैं? H2, I2 और HI के आंशिक दबाव क्या हैं?
8 विकल्प
1. जिस प्रणाली में एंडोथर्मिक गैस-चरण प्रतिक्रिया ए + 3 बी = 2 सी होती है वह 400 के और 5 एटीएम पर संतुलन में होती है। यदि गैसें आदर्श हैं, तो तापमान बढ़ाने से उत्पाद की उपज कैसे प्रभावित होगी?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 0.5 ए + 2 बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.3 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . एक 1-लीटर के बर्तन में 0.341 mol PCl5 और 0.233 mol N2 को 250°C तक गर्म किया गया। संतुलन पर पोत में कुल दबाव 29.33 एटीएम निकला। सभी गैसों को आदर्श मानते हुए, बर्तन में होने वाली प्रतिक्रिया PCl5(g) = PCl3(g) + Cl2(g) के लिए 250 °C पर संतुलन स्थिरांक की गणना करें।
9 विकल्प
1 . वह प्रणाली जिसमें एंडोथर्मिक गैस-चरण प्रतिक्रिया A+3B=2C आगे बढ़ती है, 400 K और 5 एटीएम पर संतुलन में है। यदि गैसें आदर्श हैं, तो दाब वृद्धि उत्पाद की उपज को कैसे प्रभावित करेगी?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 0.5 ए + बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोलों की संख्या 0.5 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . 500 K पर प्रतिक्रिया CO(g) + 2H2 = CH3OH(g) का संतुलन स्थिरांक है क्रू= 0.00609 ([पी] = 1 एटीएम)। यदि CO और H2 को 1:2 के अनुपात में लिया जाए तो 90% उपज के साथ मेथनॉल का उत्पादन करने के लिए आवश्यक कुल दबाव की गणना करें।
10 विकल्प
1. आंशिक दाब को मापकर साम्य स्थिरांक ज्ञात करने की विधि का वर्णन कीजिए।
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 0.5 ए + 1.5 बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.4 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . प्रतिक्रिया में संतुलन 2NOCl (g)=2NO(g)+Cl2(g) 227°C पर स्थापित होता है और 1.0 bar का कुल दबाव होता है, जब NOCl का आंशिक दबाव 0.64 bar होता है (शुरुआत में केवल NOCl मौजूद था)। दिए गए तापमान पर इस प्रतिक्रिया की गणना करें।
11 विकल्प
1 . साम्य स्थिरांक ज्ञात करने की रासायनिक विधियों का वर्णन कीजिए।
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 2 ए + 0.5 बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.2 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . कुल दबाव की गणना करें जिसे 400 डिग्री सेल्सियस पर 10 वोल्ट% एनएच 3 युक्त संतुलन मिश्रण प्राप्त करने के लिए 3 भागों एच 2 और 1 भाग एन 2 के मिश्रण पर लागू किया जाना चाहिए।
प्रतिक्रिया के लिए संतुलन स्थिरांक N2(g) + 3 H2(g)= 2NH3(g) 400°C पर
और एटीएम में दबाव की अभिव्यक्ति 1.6 10-4 है।
12 विकल्प
1 . वह प्रणाली जिसमें एंडोथर्मिक गैस-चरण प्रतिक्रिया A+3B=2C आगे बढ़ती है, 400 K और 5 एटीएम पर संतुलन में है। यदि गैसें आदर्श हैं, तो दबाव में कमी से उत्पाद की उपज कैसे प्रभावित होगी?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 2 ए + बी = 0.5 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.4 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . 250 डिग्री सेल्सियस और 1 एटीएम के कुल दबाव पर, पीसीएल 5 प्रतिक्रिया पीसीएल 5 (जी) = पीसीएल 3 (जी) + सीएल 2 (जी) के अनुसार 80% से अलग हो जाता है। यदि सिस्टम में नाइट्रोजन को जोड़ा जाता है तो PCl5 के पृथक्करण की डिग्री क्या होगी ताकि नाइट्रोजन का आंशिक दबाव 0.9 atm हो? कुल दबाव 1 बजे बनाए रखा जाता है।
13 विकल्प
1 . वह तंत्र जिसमें ऊष्माक्षेपी अभिक्रिया होती है
CO(g) + 2H2 = CH3OH(g) 500 K और 10 bar पर संतुलन में है।
यदि गैसें आदर्श हैं, तो दबाव में कमी से मेथनॉल की उपज कैसे प्रभावित होगी?
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 1.5 ए + 3 बी = 2 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोलों की संख्या 0.5 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3 . 500 K पर प्रतिक्रिया CO(g) + 2H2 = CH3OH(g) का संतुलन स्थिरांक 6.09 × 10 5 ([p] = 1 atm) है। प्रतिक्रिया मिश्रण, जिसमें सीओ का 1 मोल होता है,
H2 के 2 mol और 1 mol अक्रिय गैस (नाइट्रोजन) को 500 K तक गर्म किया जाता है और कुल दबाव 100 atm होता है। प्रतिक्रिया मिश्रण की संरचना की गणना करें।
14 विकल्प
1 . विद्युत रासायनिक डेटा से संतुलन स्थिरांक निर्धारित करने की एक विधि का वर्णन करें।
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 2 ए + 0.5 बी = सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। प्रारंभिक समय में कोई प्रतिक्रिया नहीं होती है सिस्टम में उत्पाद, और शुरुआती पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोल की संख्या 0.4 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3. प्रतिक्रिया के लिए N2 (g) + 3 H2 (g) \u003d 2NH3 (g) 298 K पर, संतुलन स्थिरांक जब एटीएम दबाव में व्यक्त किया जाता है तो 6.0 × 10 5 होता है, और अमोनिया गठन की मानक दाढ़ की थैली = - 46.1 kJ / मोल। 500 K पर संतुलन स्थिरांक का मान ज्ञात कीजिए।
15 विकल्प
1 . एक्ज़ोथिर्मिक प्रतिक्रिया CO(g) + 2H2 = СH3OH(g) वाला सिस्टम 500 K और 10 bar पर संतुलन में है। यदि गैसें आदर्श हैं, तो तापमान कम करने से मेथनॉल की उपज कैसे प्रभावित होगी।
2. गैसीय पदार्थ ए और बी का मिश्रण होता है, जो स्टोइकोमेट्रिक समीकरण 2 ए + बी = 1.5 सी के अनुसार प्रतिक्रिया उत्पाद सी के गठन के साथ रासायनिक प्रतिक्रिया में प्रवेश कर सकता है। समय के प्रारंभिक क्षण में, सिस्टम में कोई प्रतिक्रिया उत्पाद नहीं होता है, और प्रारंभिक पदार्थ स्टोइकोमेट्रिक मात्रा में लिए जाते हैं। संतुलन स्थापित होने के बाद, संतुलन मिश्रण में उत्पाद C के मोलों की संख्या 0.5 के बराबर होती है, और कुल दबाव 2 atm होता है। p-स्केल में संतुलन स्थिरांक ज्ञात कीजिए।
3. प्रतिक्रिया का संतुलन स्थिरांक N2(g) + 3 H2(g)= 2NH3(g) 400 डिग्री सेल्सियस पर और एटीएम में व्यक्त 1.6 10-4 है। नाइट्रोजन के 10% को अमोनिया में बदलने के लिए नाइट्रोजन और हाइड्रोजन के एक विषुवतीय मिश्रण पर कुल कितना दबाव लागू किया जाना चाहिए? गैसों को आदर्श माना जाता है।
प्रयोगशाला कार्य रिपोर्ट में निम्नलिखित अनुभागों को शामिल करना उचित प्रतीत होता है: परिचय, भाग 1, भाग 2, निष्कर्ष।
1 परिचय आप निम्नलिखित मुद्दों में से किसी एक पर सैद्धांतिक जानकारी संक्षेप में प्रस्तुत कर सकते हैं: या तो सामूहिक कार्रवाई के कानून पर, इसकी खोज का इतिहास और इसके लेखक; या "रासायनिक संतुलन" खंड की बुनियादी अवधारणाओं और परिभाषित संबंधों के बारे में; या इसके आधुनिक निरूपण में रासायनिक संतुलन के नियम को व्युत्पन्न करना; या उन कारकों के बारे में बात करें जो संतुलन स्थिरांक के मूल्य को प्रभावित करते हैं, आदि।
खंड "परिचय" कार्य के उद्देश्यों के विवरण के साथ समाप्त होना चाहिए।
भाग 1 ज़रूरी
2.1. धातु कार्बोनेटों के वियोजन की लोच ज्ञात करने के लिए संस्थापन का चित्र दीजिए तथा प्रयोग की प्रक्रिया का वर्णन कीजिए।
2.2 . प्रयोगात्मक डेटा के अनुसार संतुलन स्थिरांक की गणना के परिणाम दें
2.3. थर्मोडायनामिक डेटा के अनुसार संतुलन स्थिरांक की गणना दें
भाग 2 ज़रूरी
3.1 . कार्य 2 के प्रश्न 1 का पूर्ण न्यायोचित उत्तर दें।
3.2 . कार्य 2 के कार्य 2 और 3 का समाधान दें। कार्यों की स्थिति प्रतीकात्मक संकेतन में लिखी जानी चाहिए।
निष्कर्ष में कार्य में निर्धारित लक्ष्यों की पूर्ति को प्रतिबिंबित करने के साथ-साथ 2.2 और 2.3 में गणना किए गए संतुलन स्थिरांक के मूल्यों की तुलना करना उचित है।
ग्रंथ सूची सूची
1. रासायनिक ऊष्मप्रवैगिकी के करजाकिन: प्रोक। विश्वविद्यालयों के लिए भत्ता। एम.: अकादमी।, 20 एस।
2. आधुनिक ऊष्मप्रवैगिकी। ऊष्मा इंजन से लेकर विघटनकारी संरचनाओं तक। एम.: मीर, 20 एस।
3., भौतिक रसायन विज्ञान पर चेरेपोनोव। टूलकिट। येकातेरिनबर्ग: यूराल स्टेट यूनिवर्सिटी, 2003 का प्रकाशन गृह।
4. भौतिक और रासायनिक मात्राओं की संक्षिप्त संदर्भ पुस्तक / एड। तथा। एल।: रसायन विज्ञान, 20 एस।
5. भौतिक रसायन विज्ञान में कार्य: पाठ्यपुस्तक। विश्वविद्यालयों / आदि के लिए भत्ता। एम।: परीक्षा, 20 एस।
कंप्यूटर लेआउट